CHUYÊN ĐỀ 2: ĐỘ TAN – NỒNG ĐỘ DUNG DỊCH
Một số công thức tính cần nhớ:
Công thức tính độ tan: St chất =
chất =  . 100
. 100
Công thức tính nồng độ %: C% =  . 100%
. 100%
mdd = mdm + mct Hoặc mdd = Vdd (ml) . D(g/ml)
* Mối liên hệ giữa độ tan của một chất và nồng độ phần trăm dung dịch bão hoà của chất đó ở một nhiệt độ xác định.
Cứ 100g dm hoà tan được Sg chất tan để tạo thành (100+S)g dung dịch bão hoà.
Vậy: x(g) // y(g) // 100g //
Công thức liên hệ: C% =  Hoặc S =
Hoặc S = 
Công thức tính nồng độ mol/lit: CM =  =
= 

* Mối liên hệ giữa nồng độ % và nồng độ mol/lit.
Công thức liên hệ: C% =  Hoặc CM =
Hoặc CM = 
Trong đó:
- mct là khối lượng chất tan( đơn vị: gam)
- mdm là khối lượng dung môi( đơn vị: gam)
- mdd là khối lượng dung dịch( đơn vị: gam)
- V là thể tích dung dịch( đơn vị: lit hoặc mililit)
- D là khối lượng riêng của dung dịch( đơn vị: gam/mililit)
- M là khối lượng mol của chất( đơn vị: gam)
- S là độ tan của 1 chất ở một nhiệt độ xác định( đơn vị: gam)
- C% là nồng độ % của 1 chất trong dung dịch( đơn vị: %)
- CM là nồng độ mol/lit của 1 chất trong dung dịch( đơn vị: mol/lit hay M)
DẠNG 1: TOÁN ĐỘ TAN
Loại 1: Bài toán liên quan giữa độ tan của một chất và nồng độ phần trăm dung dịch bão hoà của chất đó.
Bài 1: ở 400C, độ tan của K2SO4 là 15. Hãy tính nồng độ phần trăm của dung dịch K2SO4 bão hoà ở nhiệt độ này?
Đáp số: C% = 13,04%
Bài 2: Tính độ tan của Na2SO4 ở 100C và nồng độ phần trăm của dung dịch bão hoà Na2SO4 ở nhiệt độ này. Biết rằng ở 100C khi hoà tan 7,2g Na2SO4 vào 80g H2O thì được dung dịch bão hoà Na2SO4.
Đáp số: S = 9g và C% = 8,257%
Loại 2: Bài toán tính lượng tinh thể ngậm nước cần cho thêm vào dung dịch cho sẵn.
Cách làm:
Dùng định luật bảo toàn khối lượng để tính:
* Khối lượng dung dịch tạo thành = khối lượng tinh thể + khối lượng dung dịch ban đầu.
* Khối lượng chất tan trong dung dịch tạo thành = khối lượng chất tan trong tinh thể + khối lượng chất tan trong dung dịch ban đầu.
* Các bài toán loại này thường cho tinh thể cần lấy và dung dịch cho sẵn có chứa cùng loại chất tan.
Bài tập áp dụng:
Bài 1: Tính lượng tinh thể CuSO4.5H2O cần dùng để điều chế 500ml dung dịch CuSO4 8%(D = 1,1g/ml).
Đáp số: Khối lượng tinh thể CuSO4.5H2O cần lấy là: 68,75g
Bài 2: Để điều chế 560g dung dịch CuSO4 16% cần phải lấy bao nhiêu gam dung dịch CuSO4 8% và bao nhiêu gam tinh thể CuSO4.5H2O.
Hướng dẫn
* Cách 1:
Trong 560g dung dịch CuSO4 16% có chứa.
mct CuSO4(có trong dd CuSO4 16%) =  =
=  = 89,6(g)
= 89,6(g)
Đặt mCuSO4.5H2O = x(g)
1mol(hay 250g) CuSO4.5H2O chứa 160g CuSO4
mdd CuSO4 8% có trong dung dịch CuSO4 16% là (560 – x) g
mct CuSO4(có trong dd CuSO4 8%) là  =
=  (g)
(g)
Giải phương trình được: x = 80.
Vậy cần lấy 80g tinh thể CuSO4.5H2O và 480g dd CuSO4 8% để pha chế thành 560g dd CuSO4 16%.
* Cách 2: Giải hệ phương trình bậc nhất 2 ẩn.
* Cách 3: Tính toán theo sơ đồ đường chéo.
Lưu ý: Lượng CuSO4 có thể coi như dd CuSO4 64%(vì cứ 250g CuSO4.5H2O thì có chứa 160g CuSO4). Vậy C%(CuSO4) =  .100% = 64%.
.100% = 64%.
Loại 3: bài toán tính lượng chất tan tách ra hay thêm vào khi thay đổi nhiệt độ một dung dịch bão hoà cho sẵn.
Cách làm:
- Bước 1: Tính khối lượng chất tan và khối lượng dung môi có trong dung dịch bão hoà ở t1(0c)
- Bước 2: Đặt a(g) là khối lượng chất tan A cần thêm hay đã tách ra khỏi dung dịch ban đầu, sau khi thay đổi nhiệt độ từ t1(0c) sang t2(0c) với t1(0c) khác t2(0c).
- Bước 3: Tính khối lượng chất tan và khối lượng dung môi có trong dung dịch bão hoà ở t2(0c).
- Bước 4: áp dụng công thức tính độ tan hay nồng độ % dung dịch bão hoà(C% ddbh) để tìm a.
Lưu ý: Nếu đề yêu cầu tính lượng tinh thể ngậm nước tách ra hay cần thêm vào do thay đổi nhiệt độ dung dịch bão hoà cho sẵn, ở bước 2 ta phải đặt ẩn số là số mol(n)
Bài 1: ở 120C có 1335g dung dịch CuSO4 bão hoà. Đun nóng dung dịch lên đến 900C. Hỏi phải thêm vào dung dịch bao nhiêu gam CuSO4 để được dung dịch bão hoà ở nhiệt độ này.
Biết ở 120C, độ tan của CuSO4 là 33,5 và ở 900C là 80.
Đáp số: Khối lượng CuSO4 cần thêm vào dung dịch là 465g.
Bài 2: ở 850C có 1877g dung dịch bão hoà CuSO4. Làm lạnh dung dịch xuống còn 250C. Hỏi có bao nhiêu gam CuSO4.5H2O tách khỏi dung dịch. Biết độ tan của CuSO4 ở 850C là 87,7 và ở 250C là 40.
Đáp số: Lượng CuSO4.5H2O tách khỏi dung dịch là: 961,75g
Bài 3: Cho 0,2 mol CuO tan trong H2SO4 20% đun nóng, sau đó làm nguội dung dịch đến 100C. Tính khối lượng tinh thể CuSO4.5H2O đã tách khỏi dung dịch, biết rằng độ tan của CuSO4 ở 100C là 17,4g/100g H2O.
Đáp số: Lượng CuSO4.5H2O tách khỏi dung dịch là: 30,7g
DẠNG 2: TOÁN NỒNG ĐỘ DUNG DỊCH
Bài 1: Cho 50ml dung dịch HNO3 40% có khối lượng riêng là 1,25g/ml. Hãy:
a/ Tìm khối lượng dung dịch HNO3 40%?
b/ Tìm khối lượng HNO3?
c/ Tìm nồng độ mol/l của dung dịch HNO3 40%?
Đáp số:
a/ mdd = 62,5g
Bài 2: Hãy tính nồng độ mol/l của dung dịch thu được trong mỗi trường hợp sau:
a/ Hoà tan 20g NaOH vào 250g nước. Cho biết DH O = 1g/ml, coi như thể tích dung dịch không đổi.
O = 1g/ml, coi như thể tích dung dịch không đổi.
b/ Hoà tan 26,88 lít khí hiđro clorua HCl (đktc) vào 500ml nước thành dung dịch axit HCl. Coi như thể dung dịch không đổi.
c/ Hoà tan 28,6g Na2CO3.10H2O vào một lượng nước vừa đủ để thành 200ml dung dịch Na2CO3.
Đáp số:
a/ CM( NaOH ) = 2M
b/ CM( HCl ) = 2,4M
c/ CM(Na2CO3) = 0,5M
Bài 3: Cho 2,3g Na tan hết trong 47,8ml nước thu được dung dịch NaOH và có khí H2 thoát ra . Tính nồng độ % của dung dịch NaOH?
Đáp số: C%(NaOH) = 8%
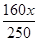


mình muốn hỏi bài tập này:
ReplyDeleteCho 4,8 gam Mgtacs dụng vừa đủ với 100 ml dd HCl.
a,Viết phương trình PUWHH.
b, tính thể tích khí o2.
c, Tinh nồng độ của axit đó dùng
d,Tính thể tích dd NaOH 10% (d=1.25 g/ml) vừ đủ để trung hòa lượng axit nói trên.
mình muốn hỏi bài tập này:
ReplyDeleteCho 4,8 gam Mgtacs dụng vừa đủ với 100 ml dd HCl.
a,Viết phương trình PUWHH.
b, tính thể tích khí o2.
c, Tinh nồng độ của axit đó dùng
d,Tính thể tích dd NaOH 10% (d=1.25 g/ml) vừ đủ để trung hòa lượng axit nói trên.
bài giải của em đây: http://www.tranganhnam.com/2016/01/tiep-tuc-huong-dan-giai-mot-so-bai-tap.html#Đạng Thị Thu Hằng
Deleteem muốn hỏi bài tập này:
ReplyDeleteCho X,Y là hai cacboxylic mạch hở có cùng số cacbon , trong đó X đơn chức, Y hai chức .
Chia hh X,Y thành 2 phần bằng nhau:
P1: tác dụng hết Na sinh ra 4,48 l khí(đktc). Đốt cháy hoàn toàn P2 thu được 13,44 lít khí CO2(đktc). tính % khối lượng mỗi chất trong hh
ngu
Deletengu
Deleteem muốn hỏi bài tập này:
ReplyDeleteCho X,Y là hai cacboxylic mạch hở có cùng số cacbon , trong đó X đơn chức, Y hai chức .
Chia hh X,Y thành 2 phần bằng nhau:
P1: tác dụng hết Na sinh ra 4,48 l khí(đktc). Đốt cháy hoàn toàn P2 thu được 13,44 lít khí CO2(đktc). tính % khối lượng mỗi chất trong hh
ngu
DeleteAi?
Deletecho dd ch3cooh a% tác dụng voi dd koh 15% thu duoc dd muoi nong do 12,5 %.tính a%?
ReplyDeleteCho 5,6g CaO vào trong 200ml H2O sau ứng thu đc dung dịch Ca(OH)2
ReplyDeletea. Tinh nồng độ mol của dung dịch Ca(OH)2
b.tinh nong do phan tram cua dung dich Ca(OH)2
Neu thay 2,3g Na vao 200ml H2O. Tinh npng do phan tram cua dung dich sau phan ung(pH2O=1g/ml
This comment has been removed by the author.
ReplyDeleteBài 2: ở 850C có 1877g dung dịch bão hoà CuSO4. Làm lạnh dung dịch xuống còn 250C. Hỏi có bao nhiêu gam CuSO4.5H2O tách khỏi dung dịch. Biết độ tan của CuSO4 ở 850C là 87,7 và ở 250C là 40. giai nhu the nao
ReplyDeleteCho mình hỏi bài này cách giải ra sao
ReplyDeleteCần hoà tan bao nhiêu gam kim loại Na vào 47,8 gam dd NaOH 25% để thu được dd có nồng độ 31,9% ?
cho em hỏi hòa tan 7.18g muối NaCl vào 20g nước ở 20C thì đc dd bão hòa. Độ tan của NaCl ở nhiệt độ đó là bao nhiêu?
ReplyDeleteCái này có nội dung giống y chang với cuốn sách mình mới mua.
ReplyDeleteCho 3.6g Mg phản ứng với dung dịch HCl 14,6 % tạo thành Muối Magie MgCl2 và khí H2.
ReplyDeletea) Viết PTHH xảy ra
b) Tính khối lượng dung dịch HCl cần dùng
Giúp em với, mai em thi rồi :(
Đang cần công thức tính nồng độ phần trăm, thanks ad
ReplyDelete