Flo
Posted on Tháng Một 7, 2008 by Phan Vinh
I. TRẠNG THÁI TỰ NHIÊN. ĐIỀU CHẾ
1. Trạng thái tự nhiên
- Tồn tại ở dạng hợp chất có trong men răng , trong lá một số cây.
- Phần lớn flo tập trung trong hai khoáng vật là florit (CaF2) và criolit (Na3AlF6 hay AlF3.3NaF)
Các mẫu khoáng vật florit
Mẫu khoáng vật criolit
- Chiếm 0.08% khối lượng vỏ trái đất.
2. Điều chế
- Phương pháp điện phân
+ Điện phân nóng chảy: hỗn hợp KF+2HF, bình điện phân có cực âm làm bằng thép đặc biệt hay đồng và cực dương bằng than chì. Khí hiđro thoát ra ở cực âm và khí flo thoát ra ở cực dương
II. TÍNH CHẤT. ỨNG DỤNG
1. Tính chất vật lí
Từ hình ảnh flo, cho biết trạng thái, màu sắc flo?
- Ở điều kiện thường, F2 là chất khí, màu lục nhạt, rất độc.
2. Tính chất hóa học:
Từ độ âm điện, cho biết tính PK? Tính oxi hoá của Flo?
-Tính oxi hóa mạnh.
2.1. Tác dung với KL: (hầu hết KL cả Pt, Au)
2.2. Tác dụng với PK ( tr ừ O2, N2) :
2.3. Tác dụng với H2
- Phản ứng xảy ra ở nhiệt độ rất thấp (-2520C)
2.4. Tác dung với H2O:
- F2 qua nước nóng là bốc cháy, giải phóng O2.
Phản ứng trên chứng tỏ tính oxi hoá của F mạnh hơn hay yếu hơn oxi?
* Kết luận: F2 là chất oxi hóa mạnh nhất trong nhóm Halogen.
Flo tác dụng được với dung dịch NaCl , đẩy clo ra khỏi muối không? vì sao?
3. Ứng dụng:
- chất oxi hoá cho nhiên liệu lỏng dùng trong tên lửa
- Teflon ( là một chất dẻo chứa flo chịu được tác dụng của axit, kiềm và các hoá chất khác).Teflon được để trám vào nồi, chảo không dính,…
- Freon ( chủ yếu là CFCl3 và CF2Cl2) được dùng trong các tủ lạnh và máy lạnh ( tuy nhiên khi được thải ra khí quyến, freon phá hủy tầng ozon gây hại môi trường. nên chúng đang được thay thế dần bằng các chất khác)
Tìm tư liệu: vật liệu thay thế freon hiện nay?
Tìm tư liệu: vật liệu thay thế freon hiện nay?
- Dung dịch NaF loãng được dùng làm thuốc chống sâu răng.
- Flo còn dùng trong công nghiệp sản xuất nhiên liệu hạt nhân để làm giàu 235U
III. MỘT SỐ HỢP CHẤT CỦA FLO
1. Hiđro florua và axit flohiđric
* Điều chế Hiđro florua
Cho canxi florua tác dụng với axit sunfuric đặc ở 2500C
* Tính chất:
- Hiđro florua có t0s=+19,50C
- Tan vô hạn trong nước, tạo thành dung dịch axit flohiđric, là một axit yếu ( so sánh với axit HCl)
- Axit HF có tính chất đặc biệt: tác dụng với SiO2( ăn mòn thủy tinh).
Nên người ta đựng axit HF trong các chai lọ bằng chất dẻo. Axit HF được dùng để khắc chữ lên thuỷ tinh (click vào đây để xem mô phỏng)
- Muối của axit flohiđric là florua. AgF dễ tan trong nước ( khác AgCl, AgBr, AgI), các muối florua đều độc.
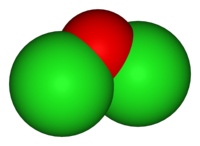
2. Hợp chất của flo với oxi: oxi florua
- Công thức: OF2
( xác định số oxi hoá của O và F)
- Điều chế: cho flo qua dung dịch NaOH loãng (khoảng 2%) và lạnh
- Oxi florua là chất khí không màu, có mùi đặc biệt, rất độc. Là chất oxi hoá mạnh, OF2 tác dụng với hầu hết các kim loại và phi kim tạo thành oxit và florua
CỦNG CỐ
Câu 1: Trong các hợp chất flo luôn có số oxi hoá âm vì flo là phi kim:
A. mạnh nhất
B. có bán kính nguyên tử nhỏ nhất
C. có độ âm điện lớn nhất
D. A, B, C đều đúng
Câu 2: Từ flo đến iot, nhiệt độ nóng chảy và nhiệt độ sôi của các đơn chất halogen biến đổi theo quy luật:
A. tăng B. không thay đổi
C. giảm D. vừa tăng vừa giảm
Câu 3: HX ( X là halgen) có thể điều chế bằng phản ứng hoá học:
NaX + H2SO4 đặc -> HX + NaHSO4
NaX có thể là chất nào trong số các chất sau đây?
A. NaCl B. NaCl hoặc NaBr
C. NaBr hoặc NaI D. NaF hoặc NaCl
Câu 4: Dung dịch nào trong các dung dịch axit sau đây không được chứa trong bình bằng thuỷ tinh?
A. HCl B. H2SO4 C. HF D. HNO3
Câu 5: Cho phản ứng: 2F2 + H2O -> 4HF + O2
Phản ứng trên cho biết:
A. flo chỉ có tính khử
B. flo chỉ có tính oxi hoá
C. flo vừa có tính oxi hoá vừa có tính khử
D. flo không có tính oxi hoá, không có tính khử
Câu 6: Ion nào không bị oxi hoá bằng những chất hoá học?
A. Cl- B. I- C. F- D. Br-
Câu 7: Những cấu hình electron nguyên tử nào là của 2 nguyên tố đầu trong nhóm VIIA?
A. 1s2 2s1 và 1s2 2s2
B. 1s2 2s2 và 1s2 2s2 2p1
C. 1s2 2s2 2p5 và 1s2 2s2 2p6 3s2 3p5
D. 1s2 2s2 2p6 và 1s2 2s2 2p6 3s2 3p5
Câu 8: Cho các muối: NaCl (1), NaBr (2), NaI (3), NaF (4). Muốn điều chế các hiđro halogen ta có thể dùng muối nào trong các muối trên cho tác dụng với H2SO4 đặc?
A. (1) và (2) B. (2) và (3)
C. (1) và (4) D. (4) và (3)
Câu 9: Dùng hoá chất nào sau đây để phân biệt natri florua và natri clorua?
A. H2SO4 đặc B. dung dịch AgNO3
C. F2 D. Cl2
Câu 10: Khoáng vật nào sau đây có chứa flo?
A. cacnalit
B. xinvinit
C. pirit
D. criolit







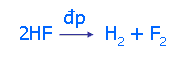
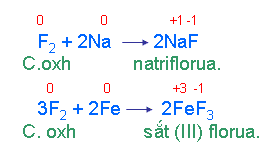


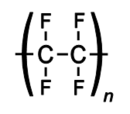





Comments
Post a Comment