Subscribe to:
Post Comments (Atom)
Bài Ðược Xem Nhiều
-
Tìm m để Phương trình: x 4 -2x 2 -m=0 có 4 nghiệm phân biệt. Đặt t=x 2 =>t>=0 Phương trình trở thành: t 2 -2t-m=0 (*) ...
-
* Công thức : Tính số số hạng của một dãy số theo quy luật ( hay tính số phần tử của một tập hợp ) ...
-
CHUYÊN ĐỀ 8: AXIT TÁC DỤNG VỚI MUỐI 1/ Phân loại axit Gồm 3 loại axit tác dụng với muối. a/ Axit loại 1: - Thường gặp là HCl, H 2...
-
PHƯƠNG PHÁP CHUẨN ĐỘ AXIT – BAZƠ I. Đặc điểm. - Dùng phương pháp này để xác định nồng độ axit, bazơ. - ...
-
B . NHỮNG HẰNG ĐẲNG THỨC ĐÁNG NHỚ 1. (A+B) 2 = A 2 +2AB+B 2 2. (A – B) 2 = A 2 – 2AB+ B 2 3. A 2 – B 2 = (A-B)(A+B) 4. (A+B) 3 = A 3 +3A 2...
-
Chuyên đề : Rút gọn biểu thức A. MỞ ĐẦU Hàng năm trong các đề thi môn toán của kỳ thi vào lớp 10- THPT phần rút gọn biểu thức thư...
-
I. Lí thuyết cơ bản. Câu 1: Lấy ví dụ về. a. 1 pứ kim loại + axit . e. 1 pứ muối + muối b. 1 pứ kim loại ...
-
CHUYÊN ĐỀ 10: HAI DUNG DỊCH MUỐI TÁC DỤNG VỚI NHAU. Công thức 1 : Muối + Muối ---> 2 Muối mới Điều kiện: - Muối phản ứng: tan ...
-
Phần IV: Hệ thức đệ quy Biên soạn: TS.Nguyễn Viết Đông Trường Đại Học Khoa Học Tự Nhiên Tp. Hồ Chí minh Toán Rời Rạc Nguyễn Vi...
-
CHUYÊN ĐỀ 6: AXIT TÁC DỤNG VỚI KIM LOẠI Cách làm: 1/ Phân loại axit: Axit loại 1: Tất cả các axit trên( HCl, H 2 SO 4 loãng, HBr,...), t...
Blog active
-
▼
2013
(2986)
-
▼
April
(504)
- Đề Thi Tốt Nghiệp THPT Môn Sinh Năm 2011
- Đáp Án Đề Thi Tốt Nghiệp THPT Môn Sinh Năm 2011
- Đề Thi Tố Nghiêp THPT Môn Sinh Năm 2009
- Đáp Án Đề Thi Tốt Nghiệp THPT Môn Sinh Năm 2009
- Đề Thi Tốt Nghiệp THPT Môn Sinh Năm 2008 - Không P...
- Đáp Án Đề Thi Tốt Nghiệp THPT Môn Sinh -Năm 2008 ...
- Đề Thi Tốt Nghiệp THPT Môn SInh - Nâm 2008 Phân Ba...
- Đáp Án Đề Thi Tốt Nghiệp THPT Môn SInh - Phân Ban ...
- Đề Thi Tốt Nghiệp THPT Môn Sinh Năm 2008 - KPB
- Đáp Án Đề Thi Tốt Nghiệp THPT Môn SInh năm 2008 - KPB
- Đề Thi Tốt Nghiệp THPT Môn Sinh Năm 2008 - PB
- Đáp Án Đề Thi Tốt Nghiệp THPT Môn Sinh Năm 2008 - PB
- Đề Ôn Kim Loại lớp 12 - Nguyễn Thị Thanh Trúc - Cuối
- Đề Ôn Kim Loại lớp 12 - Nguyễn Thị Thanh Trúc - Cuối
- Đáp Án Đề Ôn Kim Loại Lớp 12 - Nguyễn Thị Thanh Tr...
- Đề Thi Tốt Nghiệp THPT Môn Hóa - Năm 2012
- Đáp Án Đề Thi Tốt Nghiệp THPT Môn Hóa - Năm 2012
- Đề Thi Tốt Nghiệp THPT Môn Hóa Lớp 12 năm 2010
- Đáp Án Đề Thi Tốt Nghiệp THPT Môn Hóa Lớp 12 Năm 2010
- Đề Thi Tốt Nghiệp THPT Môn Hóa Năm 2008 - KPB
- Đáp Án Đề THPT Năm 2008 Môn Hóa - KPB
- Đề Thi Tốt Nghiệp THPT Môn Hóa Năm 2008 - PB - Lần 2
- Đáp Án Đề Thi Tốt Nghiệp THPT Môn Hóa Năm 2008 Lần 2
- Đề Thi Tốt Nghiệp THPT Môn Hóa Năm 2008 - PB
- Đề Thi Tốt Nghiệp THPT Môn Hóa Năm 2008 - PB
- Đáp Án Đầ Thi Tốt Nghiệp THPT môn Hóa năm 2008 - pb
- Đề Thi Tốt Nghiêp THPT Môn Hóa Năm 2007 - KPB
- Đề Thi Tốt Nghiêp THPT Môn Hóa Năm 2007 - KPB
- Đáp Án Đề Thi TN-PTTH Môn Hóa Năm 2007 - KPB
- Đề Thi Tốt Nghiệp THPT Môn Hóa Năm 2007
- Đáp Án Đề Thi TNPT Môn Hóa 2007
- TRUYỀN THUYẾT DÂN GIAN VỀ CUỘC KHỞI NGHĨA CỦA THIÊ...
- TRUYỀN THUYẾT DÂN GIAN VỀ CUỘC KHỞI NGHĨA TRƯƠNG ĐỊNH
- TRUYỀN THUYẾT DÂN GIAN VỀ “TỨ KIỆT”
- Văn phong tranh luận Văn phong tranh luận
- VĂN HỌC VIẾT TIỀN GIANG
- TỪ CỔ TIẾNG VIỆT TRONG “ĐẠI NAM QUỐC ÂM TỰ VỊ” của...
- Hướng Nghiệp
- TRUYỀN THUYẾT DÂN GIAN VỀ CUỘC KHÁNG CHIẾN CHỐNG...
- Bước đầu tìm hiểu về văn học so sánh
- Văn tế thập loại chúng sinh
- TÌM HIỂU DẤU VẾT VĂN HỌC TRUNG ĐẠI QUA MỘT TRÍCH ...
- Từ thơ chữ Hán Nguyễn Du, hiểu thêm tác giả Truyện...
- Truyện thơ Lục Vân Tiên - sự tiếp biến ba tư tưởng
- LÝ THUYẾT KỊCH NÓI HIỆN ĐẠI
- TIỂU THUYẾT “TỐ TÂM” CỦA HOÀNG NGỌC PHÁCH
- TIỂU THUYẾT “TỐ TÂM” CỦA HOÀNG NGỌC PHÁCH
- THỬ PHÂN BIỆT
- Những cây bút thơ Tiền Giang – một cõi đi về
- THIẾT KẾ HỆ THỐNG BÀI TẬP TIẾNG VIỆT VỀ CÂU THEO Q...
- Thị hiếu thẩm mỹ của các nhà thơ Trung Quốc, qua ...
- RÈN LUYỆN PHƯƠNG PHÁP HỌC VÀ THÓI QUEN HỌC TẬP C...
- MỐI QUAN HỆ GIỮA TRUYỀN THUYẾT VÀ CỔ TÍCH
- MỐI QUAN HỆ GIỮA TRUYỀN THUYẾT VÀ CỔ TÍCH
- MỐI QUAN HỆ GIỮA TRUYỀN THUYẾT VÀ CỔ TÍCH
- MỐI QUAN HỆ GIỮA TRUYỀN THUYẾT VÀ CỔ TÍCH
- MỐI QUAN HỆ GIỮA TRUYỀN THUYẾT VÀ CỔ TÍCH
- MỐI QUAN HỆ GIỮA TRUYỀN THUYẾT VÀ CỔ TÍCH
- MỐI QUAN HỆ GIỮA TRUYỀN THUYẾT VÀ CỔ TÍCH
- MỐI QUAN HỆ GIỮA TRUYỀN THUYẾT VÀ CỔ TÍCH
- MỐI QUAN HỆ GIỮA TRUYỀN THUYẾT VÀ CỔ TÍCH
- MỐI QUAN HỆ GIỮA TRUYỀN THUYẾT VÀ CỔ TÍCH
- PHÂN BIỆT TRUYỀN THUYẾT VÀ GIAI THOẠI
- PHÂN BIỆT TRUYỀN THUYẾT VÀ GIAI THOẠI
- PHÂN BIỆT TRUYỀN THUYẾT VÀ GIAI THOẠI
- “Khai song” và cõi lòng đầy trắc ẩn của Nguyễn Du
- “Khai song” và cõi lòng đầy trắc ẩn của Nguyễn Du
- HÌNH ẢNH NGƯỜI VỢ THƯƠNG CHỒNG
- TÌM HIỂU BÀI THƠ “MỜI TRẦU” CỦA HỒ XUÂN HƯƠNG
- RÈN LUYỆN PHƯƠNG PHÁP HỌC VÀ THÓI QUEN HỌC TẬP C...
- 20 ĐIỀU THẦY (CÔ) CẦN GHI NHỚ!
- ĐỀ THI THỬ ĐẠI HỌC Môn thi: TIẾNG ANH, khối D
- ĐỀ THI THỬ ĐẠI HỌC Môn : Tiếng Anh (Khối D)
- ĐỀ THI THỬ ĐẠI HỌC LẦN Môn: TIẾNG ANH; Khối D
- ĐỀ THI THỬ TUYỂN SINH ĐẠI HỌC, CAO ĐẲNG
- Đề Ôn Học Kì II Hóa 12 - Nguyễn Thị Thanh Trúc - T...
- Đáp Án Đề Ôn Học Kì II Hóa 12 - Nguyễn Thị Thanh T...
- Bộ Đề Ôn THi Đại Học Môn Sinh Học 05
- Bộ Đề Ôn Thi Đại Học Môn Sinh Học 04
- Bộ Đề Ôn Thi Đại Học Môn Sinh Học 30
- Bộ Đề Ôn Thi Đại Học 03
- Bộ Đề Ôn Thi Đại Học Môn Sinh Học 2.2
- Bộ Đề Ôn Thi Đại Học Môn Sinh Học 2.1
- Bộ Đề Ôn Thi Đại Học Môn Sinh 2
- Bộ Ôn thi Đại Học Môn Sinh Học 02
- Bộ Đề Ôn Thi Đại Học Sinh Học 1
- Bộ Đề Ôn Thi Đại Học Môn Sinh 01
- Bộ Đề Ôn Thi Sinh Học 14
- Bộ Đề Ôn Thi Đại Học Môn Sinh 13
- Bô5 Đề Ôn Thi Đại Học Môn Sinh 12
- Bộ Đề Ôn Thi Đại Học Môn Sinh 11
- Bộ Đề Ôn Thi Đại Học Môn Sinh 10
- Bộ Đề Ôn Thi Đại Học Môn Sinh 9
- Bộ Đề Ôn Ti Đại Học Môn SInh 8
- Bộ Đê Ôn Thi Đại Học Môn Sinh 7.2
- Bộ Đề Ôn Thi Đại Học Môn Sinh 7.1
- Bộ Đề Ôn Thi Đại Học Môn Sinh 6
- Bộ Đề Ôn Thi Đại Học Môn Sinh 5
- Thi Thử Đại Học Môn Sinh 2
- Thi Thử Đại Học Môn Sinh
-
▼
April
(504)

 Trang Trước
Trang Trước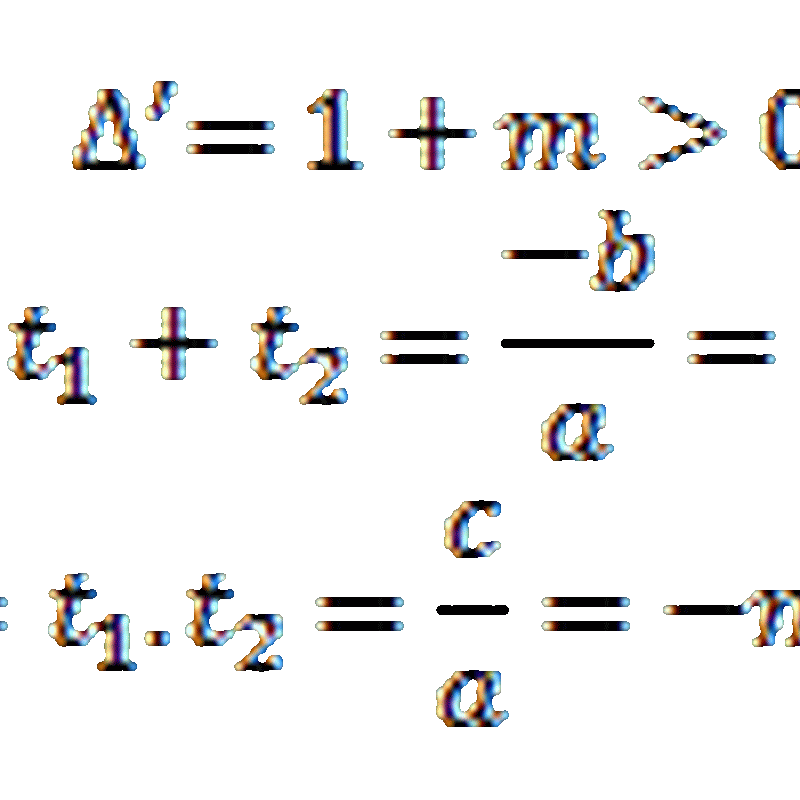







No comments: